
Eu me pergunto como nossa pesquisa vai terminar.
Parece que o tópico anterior sobre salmão OGM foi bem aceito para os habrachiters. Enquanto estamos preparando material sobre a modificação de plantas, sugiro que olhemos para um tópico igualmente interessante - a modificação genética do Homo Sapiens. Este é um tema muito controverso e holivar, que é inútil ignorar.
Darei imediatamente várias teses que podem parecer polêmicas, mas que de alguma forma precisam ser resolvidas na comunidade científica:
- Estamos degenerando. Todos os anos, indivíduos mais fracos sobrevivem, dando à luz filhos e sobrecarregando o pool genético. Isto precisa ser consertado.
- Proibições simples não ajudarão. Se os experimentos forem proibidos na Europa, então, por exemplo, a China os executará.
- Não vamos parar no tratamento de doenças genéticas. Mais cedo ou mais tarde, os militares vão se juntar aos seus super-soldados e aos que querem filhos mais fortes e inteligentes de olhos azuis.
Tentarei dar uma visão geral das técnicas de intervenção existentes no genótipo das pessoas e, ao mesmo tempo, analisaremos com o que isso nos ameaça.
O que é terapia genética
Vamos primeiro definir a terminologia. A terapia gênica é uma intervenção no genoma humano com o objetivo de tratar certas doenças. Além disso, a intervenção é apenas em células somáticas. Estas são as células que não se reproduzem. Claramente, não precisamos corrigir quaisquer mutações e correções de bugs nas novas gerações. Por enquanto, pelo menos.
Experimentos reais com animais começaram por volta da década de 1980, mas depois foram apenas tímidos passos. Não tínhamos nenhum tipo de beleza como as impressoras de DNA, expressando vetores para eucariotos.
Onde podemos realmente intervir?
Plasmídeos
Para começar, você pode deixar o núcleo da célula, que contém as informações genéticas básicas. Você pode usar plasmídeos.

1) DNA cromossômico de bactérias 2) Plasmídeos
Os plasmídeos são quase exclusivamente bacterianos. Às vezes encontrado em fungos primitivos e algumas plantas. Na verdade, este é o DNA, mas dobrado em um anel e flutuando separadamente no citoplasma. Ou seja, esse mecanismo separado para armazenar material genético. Para as bactérias, eles são muito importantes para transmitir mutações positivas, por exemplo, para “avisar os vizinhos” sobre as opções de proteção com antibióticos. O truque dos plasmídeos quando usados em humanos é que eles se desfazem por conta própria depois de algum tempo após serem introduzidos na célula. E também não afetam o principal aparato genético da célula. Ou seja, o firmware principal não será afetado.
Patching kernel
Em seguida, temos a capacidade de editar diretamente o fragmento de código no kernel. Esse é um procedimento mais invasivo e já traz o risco de inserir ou cortar de maneira incorreta um pedaço de DNA. Mas essa é praticamente a única opção para consertar radicalmente algum defeito genético sério, já que as células somáticas se dividirão e transmitirão a versão corrigida do DNA a seus descendentes.
Mitocôndria
As mitocôndrias são como reatores nucleares em uma célula. Eles consomem ácidos graxos e glicose e, na saída, marcam macroergs - substâncias com alta energia de ligação. Por exemplo, ATP. É um "combustível" universal para todas as reações ativas, por exemplo, para a operação de bombas de membrana osmótica contra um gradiente de concentração.
Eles têm uma peculiaridade - seu próprio aparato genético. Na verdade, eles parecem simbiontes semi-autônomos por esse motivo. Seu aparato genético faz sentido para controlar as mutações congênitas no DNA mitocondrial. Normalmente, essas também são síndromes congênitas muito graves.
O vetor viral é como uma seringa
O primeiro ponto chave é o desenvolvimento de ferramentas de distribuição - vetores virais. O primeiro desses vírus para mamíferos foi desenvolvido em 1984. Um retrovírus murino foi usado como uma seringa molecular. Ele em si era uma ferramenta muito desagradável, pois com grande probabilidade provocava doenças oncológicas. Na verdade, seu segundo nome é vírus da leucemia murina (MLVs). No futuro, o desenvolvimento mudou para opções mais seguras.
O que exatamente é um vetor viral? Este é um vírus especialmente modificado que só funciona uma vez. Como uma seringa. Para fazer isso, ele deve atender a vários critérios:
Segurança
O vetor viral não deve ser capaz de se multiplicar espontaneamente. Para isso, eles têm um interruptor de eliminação embutido. Seu genoma é inicialmente tão danificado que eles não podem se reproduzir de forma autônoma. Em um ambiente de laboratório, eles se multiplicam em cultura de células apenas na presença de componentes insubstituíveis e vírus auxiliares adicionais que produzem parte das proteínas necessárias para a montagem. Ou seja, ela se multiplica em um frasco de cultura de laboratório, mas no corpo funciona uma vez, sai da célula semi-montada e morre.
Baixa citotoxicidade
Muitos vírus são muito cruéis com as células hospedeiras. Após a fase de incubação, a célula morre de exaustão e novos vírions se espalham de seus restos mortais em todas as direções. Ao mesmo tempo, existem vírus que não afetam particularmente a fisiologia normal das células nas quais parasitam. Por exemplo, adenovírus.
Estabilidade
Os vírus devem ser geneticamente estáveis. Por exemplo, a gripe não funciona. Ele não possui nenhum mecanismo inteligível de "paridade" e não se importa se o hash após a cópia não convergiu. Esta é sua estratégia evolutiva. Os mesmos coronavírus, ao contrário, possuem mecanismos de controle e reparo, o que confere maior estabilidade do material genético. Embora não sejam usados como vetor por outros motivos. Assim, a tarefa é garantir que o vírus em processo de sua reprodução em biorreatores retenha a mesma carga útil - a carga útil inalterada.
Especificidade do tipo de célula
O vírus deve entregar sua carga não apenas em qualquer lugar, mas exatamente em um tipo específico de células. Isso significa que, se precisamos curar uma doença associada a eritrócitos defeituosos, o vírus deve infectar com muita precisão as células-tronco precursoras multipotentes das células sanguíneas. E, ao mesmo tempo, não enganchar, por exemplo, tecido muscular.
O que já está sendo feito em termos de terapia gênica
A primeira correção genética humana foi realizada em 1990. Ashanti DeSilva, de 4 anos, recebeu tratamento para um defeito genético grave de imunodeficiência combinada complexa associada a uma deficiência da enzima ADA. Deve-se notar que não foi o genoma das células-tronco que produzem os linfócitos T que foram editados, mas as células T adultas de seu próprio sangue de doador. Ou seja, ela precisava repetir esses procedimentos no futuro. Em seguida, houve uma série de protocolos experimentais bem-sucedidos para o tratamento de SCID (Imunodeficiência combinada severa) usando uma técnica semelhante.
Em 1999, ocorreu um incidente que desacelerou significativamente as pesquisas nesta área. Jesse Gelsinger, sofria de uma doença hepática genética devido à qual ela não conseguia desintoxicar a amônia. 4 dias após a introdução de um vetor adenoviral com uma cópia saudável do gene, ele morreu como resultado de uma resposta hiperimune e falência de múltiplos órgãos. Posteriormente, o FDA concluiu que havia inúmeras violações no protocolo do estudo.
Em 2006, surgiram os primeiros relatos de protocolos de terapia gênica individual bem-sucedidos para o tratamento de oncologia. As células T assassinas são programadas para um tipo específico de tumor e então liberadas no corpo do paciente. Terapia de HIV reconhecida
em 2011 no paciente Gero Hütter em 2008. O método não é particularmente aplicável a um público amplo, pois requer a remoção completa da medula óssea e, em seguida, o implante de células corrigidas com uma mutação delta-32 dupla que desativa o receptor CCR5.
Em 2013, havia apenas cinco medicamentos genéticos licenciados no mundo. Três da oncologia, glybera para o tratamento da deficiência hereditária de lipoproteína lipase e neovasculgen. Este último, aliás, foi totalmente desenvolvido por nós.
Neovasculgen
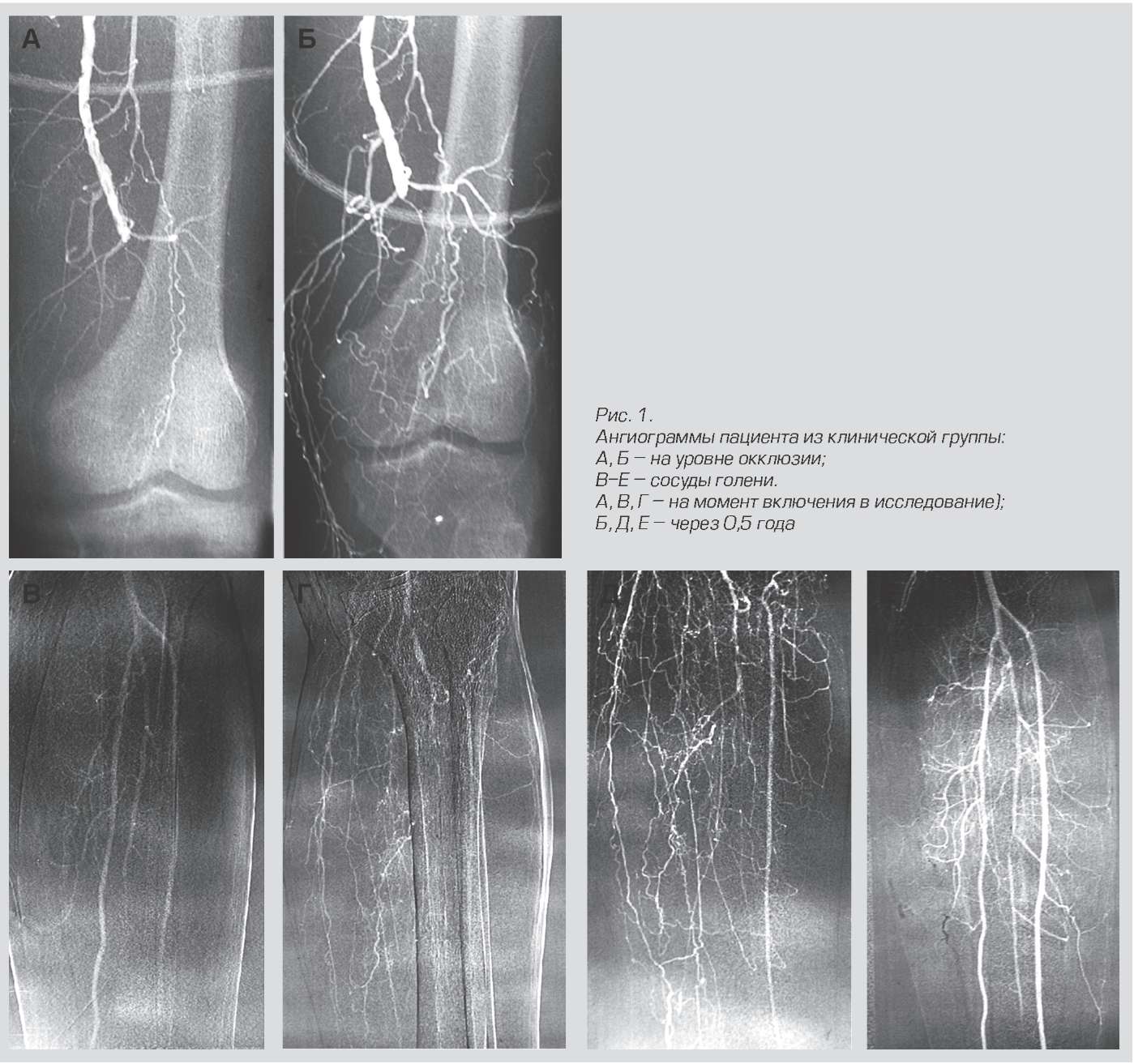
Resultados do tratamento com Neovasculgen.
Essa droga pertence ao plasmídeo, ou seja, não edita o próprio genoma da célula, mas apenas entrega plasmídeos que funcionam por um tempo limitado.
(), VEGF 165, (VEGF — Vascular Endothelial Growth Factor). , . , , .
Human Stem Cell Institute
O mecanismo de ação é interessante. As células no local da injeção começam a sintetizar VEGF, um fator de crescimento vascular. Como resultado, uma nova rede capilar ramificada começa a crescer nesta área. Isso é crítico para pacientes com isquemia crônica de membros inferiores devido ao diabetes e aterosclerose, por exemplo. Antes dessa droga, havia mais amputações. Agora também foi testado para uso em odontologia para enxerto de implantes. A preparação do gene é misturada ao material ósseo e suturada. Como resultado, os vasos crescem rapidamente e o tecido necessário é formado sem rejeição. Os coelhos já foram simulados com precisão durante o transplante de fragmentos de crânio. As pessoas são as próximas, pelo que eu sei.
Zolgensma
A atrofia muscular espinhal é uma doença muito grave, clinicamente um tanto semelhante à esclerose lateral amiotrófica que Hawking sofreu, mas tem outras causas. Como resultado do desenvolvimento da doença, progride a paralisia, que termina em morte devido à incapacidade de respirar.
Zolgensma é o primeiro medicamento de terapia genética para atrofia muscular espinhal. Produzido por AveXis (Novartis). Uma cópia de trabalho do gene SMN é injetada usando o vírus adeno-associado (AAV) do sorotipo 9, AAV9, que é capaz de cruzar a barreira hematoencefálica e entrar nas células do paciente. Um problema - custa dinheiro absolutamente monstruoso. Uma injeção custa mais de US $ 2,1 milhões (cerca de 152 milhões de rublos). Mas os resultados também são surpreendentes. Em humanos, a função motora é restaurada e a doença não progride mais. Em teoria, essas manipulações caras deveriam ser pagas pelo estado. Para os indivíduos, o custo do tratamento de doenças raras é simplesmente proibitivo.
Qual é o próximo?
Aqui está uma pergunta muito difícil. Acumulamos genes defeituosos na população. Anteriormente, uma criança com um defeito cardíaco simplesmente morreria - agora eles vão salvá-la e ela dará uma prole com esse defeito. Anteriormente, muitas gravidezes não duravam - agora as mulheres grávidas são retiradas com uma porcentagem mínima de abortos e são concluídas com partos bem-sucedidos. Na verdade, estamos quebrando os mecanismos de seleção natural da população. Isso é correto e humano, mas algo deve ser feito com o acúmulo de mutações no pool genético.
Ou chegaremos aos green cards e às licenças de reprodução ou aprenderemos como corrigir anormalidades genéticas de maneira confiável e segura. Seria legal descartar miopia, displasia sistêmica do tecido conjuntivo e um monte de outros defeitos de nascença. E, finalmente, conserte aquele gene quebrado estúpido responsável pela síntese da vitamina C a partir da glicose, como todos os mamíferos normais.
Aqui, apenas um futuro desconhecido nos espera mais. O mais alarmante é a estratificação potencial da sociedade, quando os segmentos mais ricos da população modificam seus filhos para ficarem livres do diabetes, da aterosclerose e, ao mesmo tempo, esmagam um pouco de miostatina para torná-los atléticos sem muito esforço. Legal. Mas assusta.
