
A cada ano, a linha entre o homem e a máquina fica mais tênue. Claro, o nível de "Deus Ex" ainda está longe, mas agora existem vários tipos de próteses, de aumento e outros dispositivos que funcionam em estreita ligação com o sistema nervoso do usuário. Um dos exemplos mais claros desse futurismo é o NCI (interface do neurocomputador), que garante a troca de informações entre o cérebro e o computador. O problema é que para a operação completa do NCI, uma pequena atualização é necessária por parte do usuário - a implantação de eletrodos no cérebro. Parece muito sinistro do que realmente é, mas nem todos consideram esse método o mais eficaz. Cientistas do Instituto de Tecnologia da Califórnia (EUA) desenvolveram um sistema que lê a atividade cerebral por meio de um método não invasivo baseado em ultrassom. Como funciona exatamente o dispositivo criado,O que os cientistas conseguiram ver nos cérebros das cobaias e quão preciso é esse desenvolvimento? Encontraremos respostas para essas perguntas no relatório dos cientistas. Vai.
Base de pesquisa
A essência da interface do neurocomputador é bastante simples - ler a atividade neural do cérebro humano para entender suas intenções. As informações obtidas podem ser utilizadas como sinais para controle de dispositivos neuroprotéticos. Falando exageradamente, com a ajuda do NCI, uma pessoa pode controlar tanto o cursor do mouse (sem o próprio mouse) quanto uma prótese eletrônica com o poder do pensamento.
É na área da prótese que essa tecnologia mais chama a atenção. Pois nem sempre é possível usar próteses que leem sinais de terminações nervosas na área de contato ou sinais de atividade muscular. LCI permite que você faça sem intermediários periféricos e conecte diretamente o usuário (ou seja, o cérebro) e o dispositivo.
As interfaces neurais mais modernas são baseadas na eletrofisiologia intracortical (dentro do córtex cerebral), que fornece acesso direto aos sinais elétricos dos neurônios com excelente resolução temporal. O problema dessa técnica é a necessidade de implante de eletrodos, que é feito por meio de cirurgia aberta de cérebro. É óbvio que tais procedimentos têm consequências graves na forma de danos crônicos aos tecidos e destruição do material do implante. Além disso, os eletrodos invasivos são difíceis de dimensionar e têm uma densidade de amostra limitada e, portanto, não podem capturar toda a atividade cerebral.
Uma solução lógica para esse problema é o desenvolvimento de um método não invasivo de conectar o dispositivo ao cérebro. Uma das opções é a eletroencefalografia não invasiva (EEG), que está em desenvolvimento desde 1973. No entanto, o desempenho do EEG é limitado pela representação topográfica da atividade de grandes volumes cerebrais e pela dispersão do sinal de condutância de volume através de vários tecidos e ossos.
No trabalho que estamos considerando hoje, os cientistas propõem uma alternativa na forma de NCI com base na imagem de ultrassom funcional (fUS de ultrassom funcional) O fUS permite a visualização de alterações regionais no volume sanguíneo usando a angiografia Doppler ultrarrápida. Este método fornece excelente resolução espaço-temporal (<100 μm e 100 ms) e alta sensibilidade (velocidade ~ 1 mm / s) com um grande campo de visão (vários centímetros, o que é bastante para tais dispositivos).
O fUS foi desenvolvido em 2011. Desde então, tem sido freqüentemente usado para visualizar a atividade neural durante crises epilépticas, processar estímulos olfativos e realizar tarefas comportamentais em roedores. Experimentos também foram realizados com pombos, furões e primatas. Além disso, fUS é 5-10 vezes melhor em termos de resolução espaço-tempo e sensibilidade em comparação com fMRI (de ressonância magnética funcional, ou seja, ressonância magnética funcional), devido à qual você pode obter muito mais informações sobre a atividade do cérebro.
No decorrer do estudo, experimentos foram realizados com dois macacos experimentais: um foi treinado para realizar sacadas (movimentos oculares agudos) para focar em um objeto (rastrear figuras na tela), e o segundo foi treinado para realizar certos movimentos de memória (controle uma alavanca). Em experimentos práticos, os cientistas leram a atividade neurovascular sobre o córtex parietal posterior (PPC para córtex parietal posterior ) por meio de uma janela craniana minimamente invasiva.
Por que exatamente o córtex parietal posterior? Esta área é uma zona de associação localizada entre as regiões do córtex visual e motor. Ela está ativamente envolvida em funções cognitivas de alto nível, incluindo atenção espacial, integração multissensorial e transformações sensório-motoras para planejamento de movimento. O próprio PPC pode ser dividido em subáreas funcionalmente específicas: área intraparietal lateral (LIP da área intraparietal lateral ) - planejamento do movimento ocular (quando vamos olhar para algo); região parietal de captura (PRR da região de alcance parietal ) - planejamento do movimento de captura de um objeto (quando vamos pegar algo).
Os cientistas observam que o fUS permite que você visualize simultaneamente as duas sub-regiões (LIP e PRR), ou seja, eles estarão dentro de um quadro (volume de corte aproximado de 12,8 x 13 x 0,4 mm). Além disso, como o PPC codifica aspectos de alto nível do planejamento de movimento, é uma fonte exclusiva de sinais de controle antes do movimento real.
Preparação para pesquisa
Um transdutor (transdutor) miniatura com uma matriz linear de 128 elementos (15 MHz) foi instalado periduralmente (sobre a dura-máter) através da janela craniana. Este sensor forneceu imagens fUS que servem como base para a análise de sinais neurovasculares em PPC relacionados à tarefa em questão. O transdutor forneceu uma resolução espacial de 100 x 100 µm no plano, uma espessura de corte de ~ 400 µm, cobrindo um plano com uma largura de 12,8 mm e uma profundidade de penetração de 16 mm.
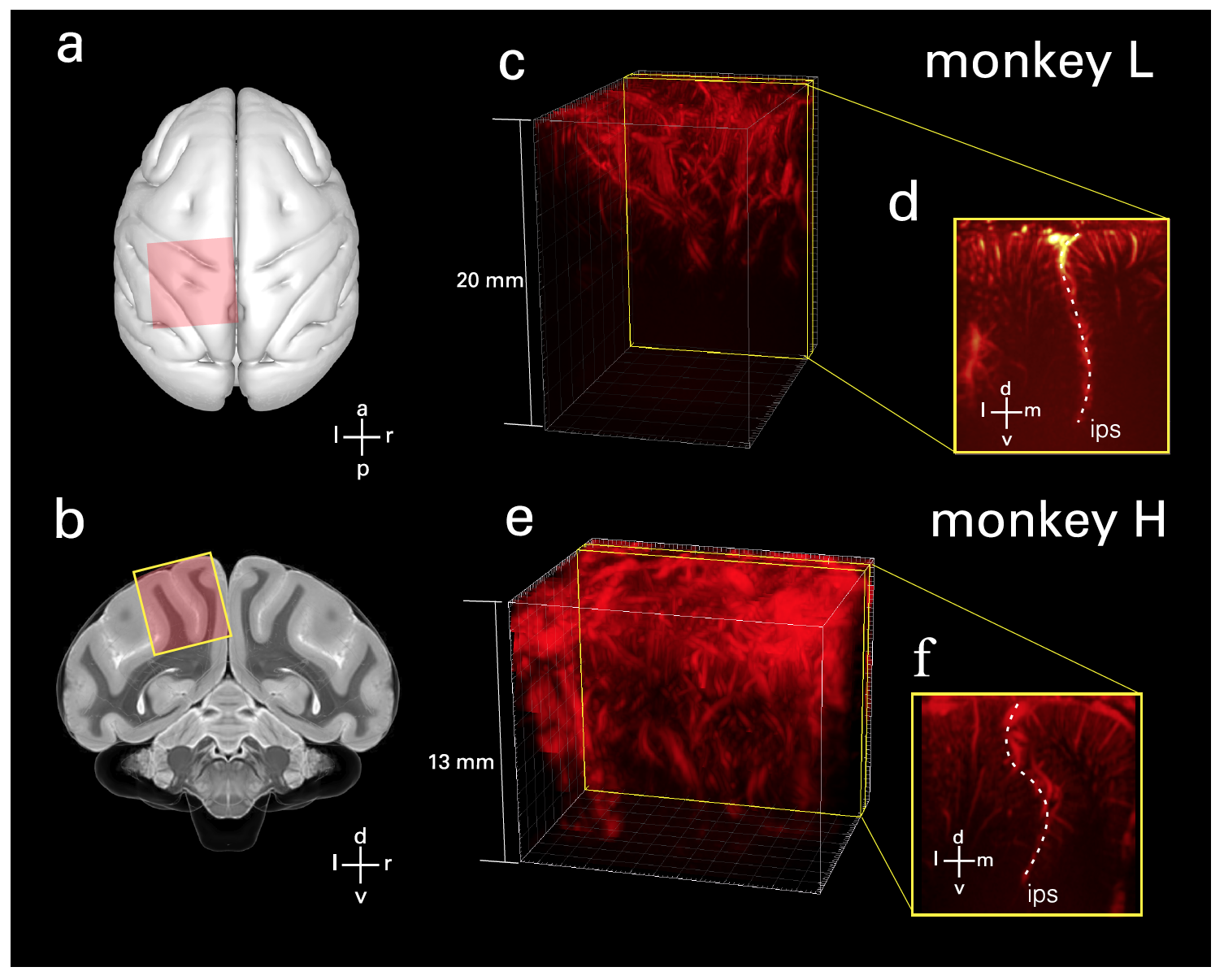
Imagem # 1 A
sonda foi posicionada perpendicularmente à superfície em uma orientação coronal na dura-máter sobre o PPC ( 1a e 1b ). Além disso, a partir dos volumes disponíveis, os planos de interesse foram selecionados ( 1c- 1f ).
Especificamente, foram selecionados planos que exibiam atividade hemodinâmica (movimento sanguíneo) ajustada comportamentalmente e capturavam os lados lateral e medial do sulco intraparietal (IPS do sulco intraparietal ; coordenação sensório-motora) em uma única imagem. Isso tornou possível avaliar as funções de várias áreas do cérebro simultaneamente. E a geometria da imagem do ultrassom permitiu o acesso às áreas corticais nos sulcos.
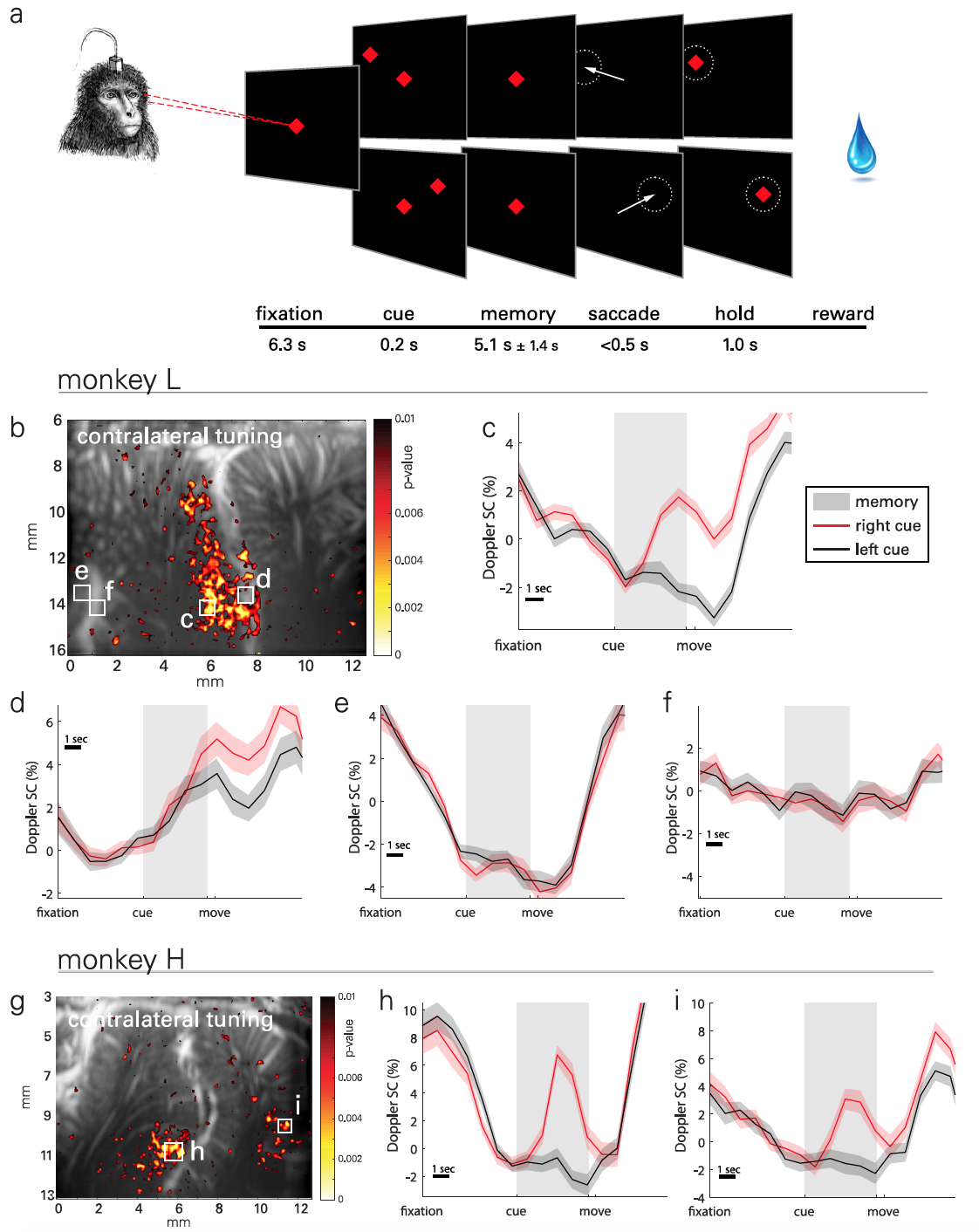
Imagem No. 2
A essência dos experimentos práticos era que os macacos tinham que memorizar a localização do objeto localizado no lado esquerdo ou direito da tela e realizar o movimento após o objeto no centro da tela sair ( 2a ). A fase de memorização foi longa o suficiente (5,1 ± 1,4 s) para registrar a hemodinâmica transitória. No total, os dados foram coletados de 30 execuções de teste realizadas ao longo de 18 dias. Até 5 execuções foram realizadas a cada dia, cada uma incluindo metas de 30 minutos geradas aleatoriamente para uma tarefa.
Para visualizar os padrões espaço-temporais de atividade lateralizada em PPC ( 2b ), mapas paramétricos estatísticos foram usados com base no teste t de Student ( exemplo de cálculo do teste t de Student ).
O resultado observado associado a tarefas médias (ERA da média relacionada ao evento ) alterações no volume de sangue cerebral (CBV do volume de sangue cerebral ) das regiões localizadas de tamanho 100 x 100 mm ( 2c - 2f ). A foto 2g mostra um mapa típico da atividade do segundo sujeito, e 2h - 2i de sua ERA.
Sinais de atividade neurovascular foram observados na face lateral do IPS, ou seja, no LIP, para ambos os animais. No entanto, as formas de onda ERA foram semelhantes entre os assuntos nesta área.
FUS de alta sensibilidade e resolução espaço-temporal permitem distinguir funções entre regiões adjacentes em uma escala de centenas de mícrons, por exemplo, dentro de sub-regiões PPC, como LIP.
Por exemplo, a segunda região LIP ( 2d ) também mostra sintonização contralateral, mas a diferença na atividade surge mais tarde no período de memorização e persiste durante o movimento e entre os experimentos.
Um sujeito (macaco H) mostrou uma resposta direcional semelhante na região parietal medial (MP de parietal medial ) na parede medial do hemisfério. Mas no macaco L, esse efeito não foi encontrado, pois no caso dela a localização da sonda foi otimizada para a região LIP, e não para o MP, que neste caso estava fora da tela. No entanto, essa configuração confirma ainda mais o papel do MP no movimento ocular direcional.
Processo de decodificação de sinal
Antes de considerar os resultados de experimentos práticos, os cientistas são lembrados de que a principal tarefa do NKI é prever a próxima ação pretendida usando sinais cerebrais. Para entender se a visualização do fUS ajuda a realizar essa tarefa, a previsão da direção do movimento ocular do sujeito foi realizada com base em um teste.
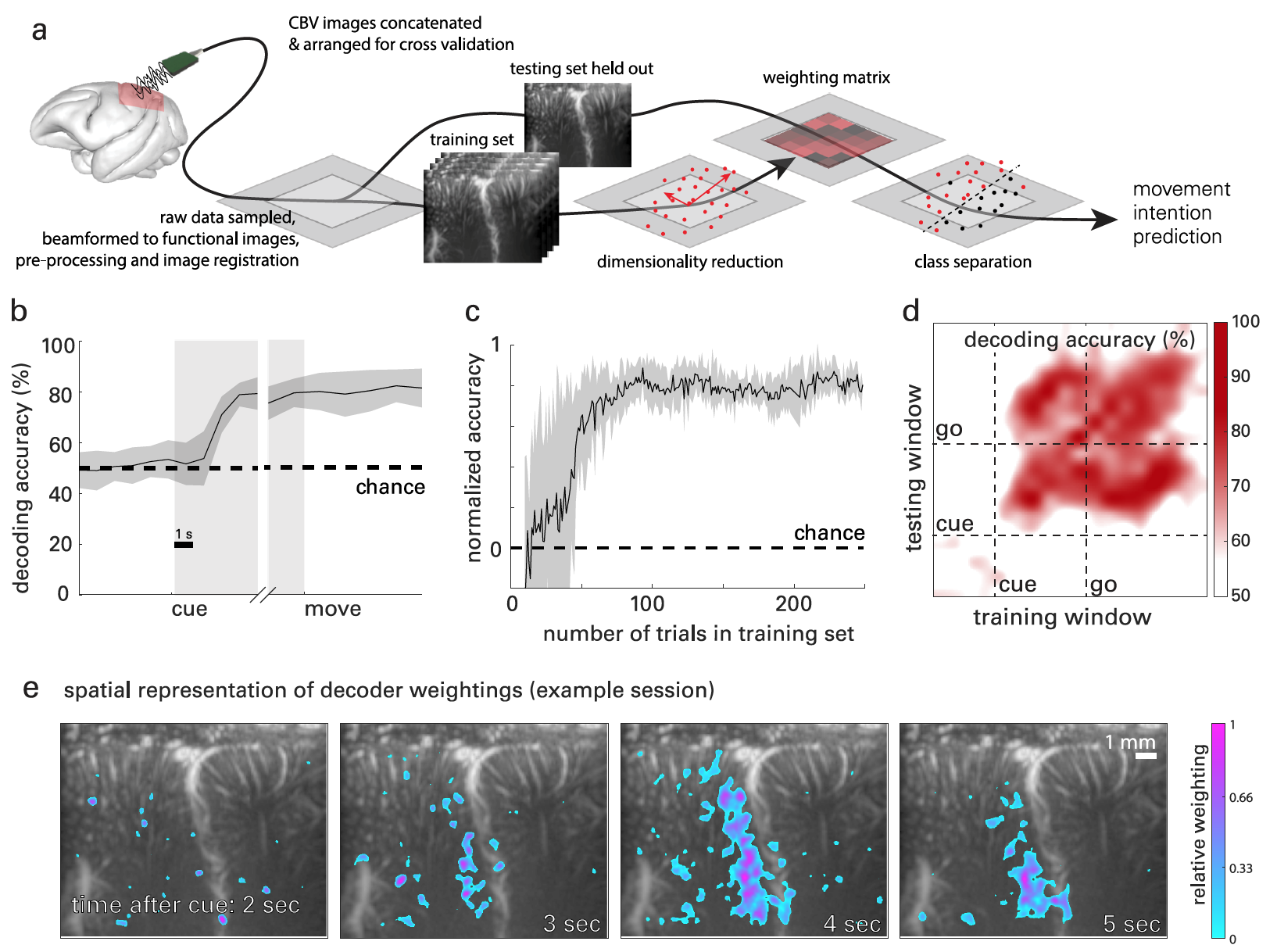
Imagem # 3 A
Figura 3a mostra uma interpretação gráfica do processo de decodificação do sinal do cérebro com base em dados fUS. A análise de componentes principais Classwise (CPCA ) foi usada para reduzir a dimensionalidade * dados, mas retendo componentes suficientes para obter> 95% da variância nos dados.
A redução de dimensão * é um processo de transformação de dados em que o número de variáveis é reduzido pela obtenção das variáveis principais.Em seguida, a regressão de mínimos quadrados ordinários (OLSR ) foi usada para regredir os dados transformados por PCA antes da execução real do movimento.
Para analisar a evolução temporal dos sinais PPC associados à execução de uma tarefa, a direção do movimento no tempo foi decifrada através das etapas de cada abordagem experimental: fixação (olhar para o objeto central), memorização e movimento.
Para cada ponto de tempo, todos os dados anteriores de treinamento e dados de teste foram usados. Por exemplo, em t = 2 s, foi necessário incluir todos os dados nos conjuntos de dados de treinamento e teste em t = de 0 a 2 s.
As curvas resultantes ( 3b ) mostrar a precisão no nível de aleatoriedade durante a fase de fixação, pequenas alterações durante a fase de armazenamento e precisão de decodificação estável durante a fase de movimento.
Durante a fase de memorização, a precisão do decodificador atingiu 2,08 s ± 0,82 s depois que o sujeito recebeu o sinal de direção, mas antes do movimento real. No futuro, a precisão do decodificador só aumentou.
A reanálise removeu todos os dados do conjunto de treinamento. Isso tornou possível determinar a quantidade de dados necessária para atingir a precisão máxima de decodificação ( 3c) Após 27 execuções de teste, a precisão do decodificador tornou-se tal que os dados de apenas 10 execuções de treinamento eram necessários para a previsão e classificação subsequente do movimento. O nível máximo de precisão do decodificador foi alcançado após 75 execuções de teste.
Em outras palavras, os cientistas foram capazes de minimizar a quantidade de dados necessários para reconhecer com precisão os sinais do cérebro, enquanto o nível de precisão desse processo permaneceu bastante alto.
Além disso, foi realizada uma análise para determinar que tipo de informação está contida nos sinais cerebrais usados pelo decodificador. Para isso, foi utilizado o método de decodificação dinâmica, que requer dados por um período de 1 segundo para treinar o decodificador. Além disso, a direção assumida foi decodificada a partir das janelas de dados com uma duração de 1 s durante toda a execução do teste. Ou seja, o decodificador tinha que entender o que o macaco faria, analisando os dados de um período de apenas 1 segundo.
Como resultado, foi obtida uma matriz de valores de precisão nxn, onde n é o número de janelas de tempo verificadas. 3d mostra a precisão de cada combinação de aprendizagem / decodificação.
Resultado dos testes
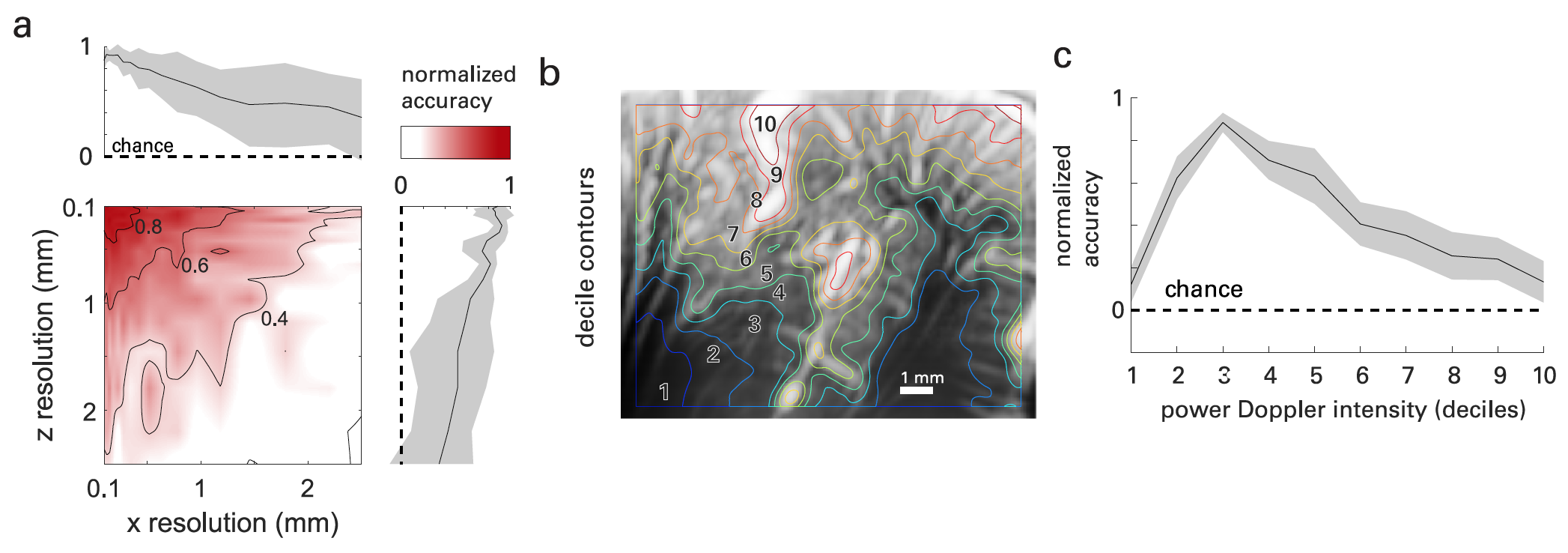
Imagem # 4
fUS fornece alta resolução espaço-temporal e sensibilidade, em contraste com o método fMRI. Isso fornece dados sobre a dinâmica neurovascular em uma escala anteriormente inacessível.
Foi fácil verificar isso. Se mudarmos as dimensões (em x - isto é, ao longo da superfície da sonda e em z - ou seja, na profundidade da imagem) das imagens obtidas durante os experimentos, a precisão da decodificação diminuirá com o aumento de o tamanho dos voxels ( 4a ).
Estudos recentes mostraram que a hiperemia funcional começa em uma região vascular chamada unidade primária. Esta seção inclui arteríolas parenquimatosas (pequenas artérias na frente dos capilares) e capilares, ou seja, vasos com diâmetro <50 μm. Conseqüentemente, a velocidade do fluxo sanguíneo aumenta nos capilares inferiores e nas arteríolas superiores.
Com isso em mente, os cientistas decidiram que a maior parte das informações funcionais usadas para decodificação seriam encontradas em vasos com subresolução (<100 μm) no plano da imagem. Para testar essa hipótese, os mapas fUS vasculares do cérebro foram segmentados (espacialmente) ordenando os voxels de acordo com sua intensidade Doppler média e segmentando-os por decis * ( 4b ).
O decil * caracteriza a distribuição dos valores da população, em que nove valores do decil a dividem em dez partes iguais. Qualquer uma dessas dez partes é 1/10 do total.Enquanto os decis 1–2 envolvem principalmente as regiões subcorticais, os decis 3–8 envolvem as camadas corticais, onde as camadas mais superficiais mostram uma intensidade média mais alta. Os decis 9 e 10 estavam confinados principalmente à vasculatura das unidades primárias (grandes artérias, geralmente na superfície cortical e nos sulcos). Em 4c mostra a precisão resultante da decodificação de acordo com a intensidade de potência Doppler.
A análise dos dados mostrou que a atividade neurovascular durante uma tarefa, medida por fUS, existe principalmente na anatomia dos vasos localizados no córtex cerebral. Ou seja, a maior contribuição para os sinais fUS corticais foi dada por velocidades de fluxo axial na faixa de 2 a 10 mm / s, que corresponde a vasos com diâmetro <50 μm, ou seja, nomeadamente arteríolas e capilares.
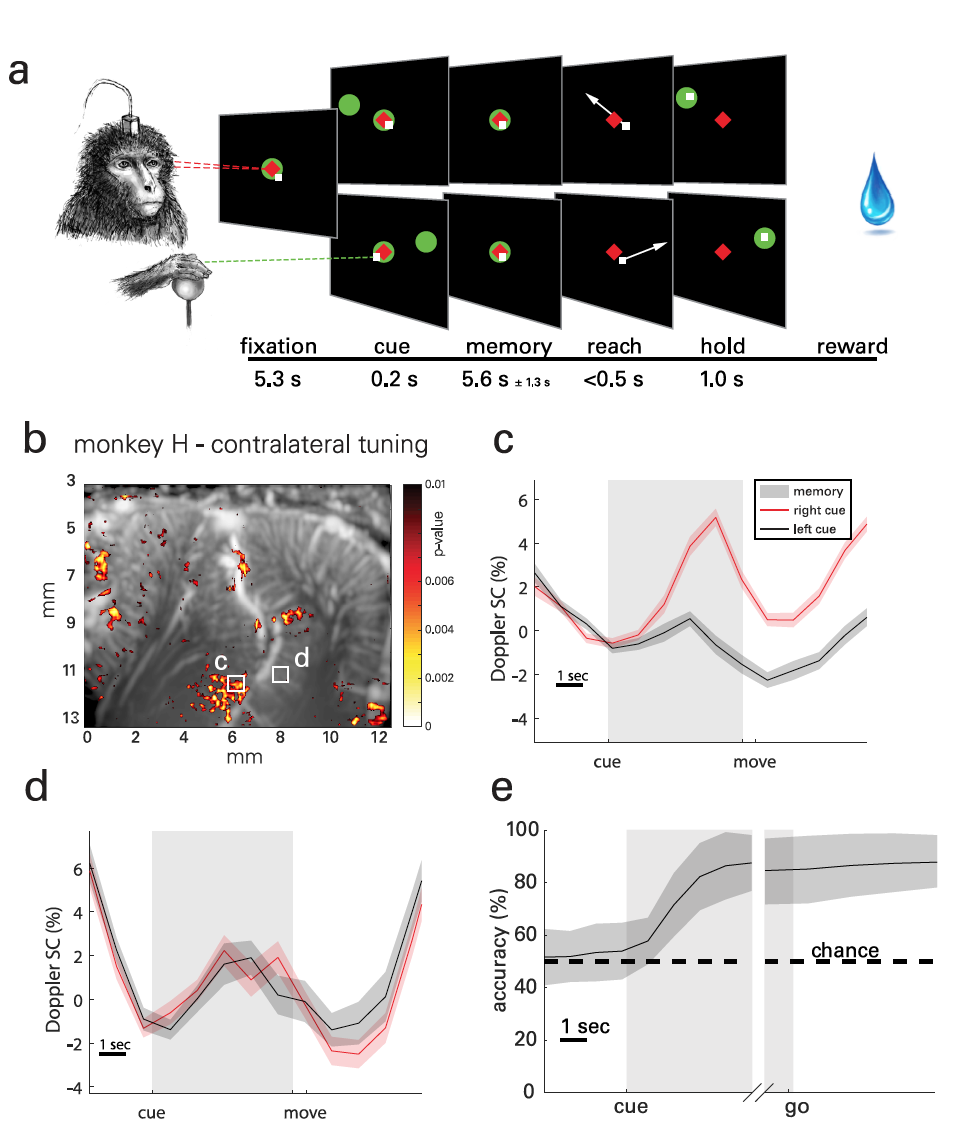
Imagem # 5 Por fim
, foi realizado outro teste no qual o sujeito tinha que operar uma alavanca enquanto olhava para os objetos na tela ( 5a ). Essa tarefa era em muitos aspectos semelhante à tarefa de sacadas, mas o olhar do animal permaneceu fixo durante todo o teste, inclusive durante as fases de fixação, memorização e execução do movimento.
ERAs (alterações médias relacionadas à tarefa) no lado lateral do sulco intraparietal no LIP putativo (região intraparietal) identificam populações relevantes para prever a direção do movimento ( 5b - 5c ). As populações do lado medial na área de retenção parietal putativa (PRR) não exibem essas características, mas exibem uma sintonia bilateral com o movimento real ( 5d ).
Esses resultados são consistentes com os registros eletrofisiológicos nos quais os neurônios PRR, como uma população, codificam ambos os hemisférios, enquanto os neurônios LIP codificam principalmente o espaço contralateral.
A precisão da decodificação e sua evolução temporal foram semelhantes às observadas em experimentos com sacadas ( 5e ). Especificamente, a precisão da decodificação do alvo validado cruzado variou de 72,96% a 94,64% em um teste de 30 minutos. A precisão média para todas as sessões experimentais foi de 88,54%.
Para um conhecimento mais detalhado das nuances do estudo, recomendo que você leia o relatório dos cientistas .
Epílogo
As interfaces de neurocomputadores, apesar do conceito futurista, estão se tornando mais reais a cada ano. Suas funcionalidades, características e capacidades estão se expandindo, assim como a gama de aplicações possíveis. No entanto, como acontece com qualquer tecnologia relativamente nova, os problemas não podem ser evitados.
Um dos principais problemas na implementação de um NKI completo é a necessidade de uma conexão invasiva. Poucas pessoas desejam mudar de canal, por exemplo, se for necessário abrir o crânio e inserir alguns elétrons no cérebro. E não se trata nem mesmo do incômodo de um tal "acessório" de cabeça, mas dos perigos que ele carrega. O método invasivo de conectar o NKI leva a violações sistemáticas da estrutura do tecido e à destruição do material do próprio dispositivo.
A solução para esse problema é a imagem de ultrassom funcional (fUS), que permite rastrear a atividade cerebral nessas áreas com incrível precisão com resolução de até 100 mícrons. E isso é realmente impressionante, considerando que o tamanho de um neurônio é de aproximadamente 10 mícrons.
Os autores desta técnica afirmam que sua criação é muito mais produtiva do que outros métodos. Os eletrodos implantados podem medir com muita precisão a atividade do cérebro no nível de neurônios individuais, mas requerem contato direto com o cérebro. A fMRI (ressonância magnética funcional) não requer implantação e pode mostrar a atividade do cérebro inteiro de uma só vez, mas o equipamento para esse método ocupa uma sala inteira. A eletroencefalografia também não requer a introdução de eletrodos, mas sua resolução espacial é extremamente baixa. Mas o método fUS, de acordo com os cientistas, é desprovido das desvantagens acima.
O princípio do fUS é baseado no fluxo sanguíneo no cérebro. Quando a atividade em uma área do cérebro aumenta, o fluxo sanguíneo para ela aumenta. O fUS permite que isso seja monitorado ao fornecer uma dinâmica de alta resolução do fluxo sanguíneo cerebral no espaço e no tempo. A análise dos dados do fluxo sanguíneo permite que você descubra quais áreas estão ativas em um determinado momento.
A precisão do fUS neste estágio de desenvolvimento é muito próxima ao método com eletrodos implantados. Mas, ao contrário deste último, o fUS não precisa de implantação completa. Para trabalhar com eletrodos, é necessário abrir a dura-máter localizada sob o crânio e inserir os eletrodos diretamente no cérebro. No caso do FUS, uma pequena janela capaz de transmitir o ultrassom é suficiente. No momento, essa janela é feita abrindo o crânio, mas sem nenhuma intervenção no próprio cérebro. Essa opção é significativamente menos invasiva e, portanto, menos perigosa.
No futuro, os cientistas pretendem continuar a aprimorar o fUS para obter uma precisão ainda maior, além de realizar experimentos em pessoas que, devido a lesões cerebrais, foram submetidas a trepanação de parte dos ossos do crânio.
Obrigado pela atenção, fiquem curiosos e tenham um ótimo final de semana galera! :)
Um pouco de publicidade
Obrigado por ficar com a gente. Você gosta de nossos artigos? Quer ver um conteúdo mais interessante? Apoie-nos fazendo um pedido ou recomendando a amigos VPS em nuvem para desenvolvedores a partir de US $ 4,99 , um análogo exclusivo de servidores básicos que inventamos para você: The Whole Truth About VPS (KVM) E5-2697 v3 (6 núcleos) 10GB DDR4 480GB SSD 1Gbps a partir de US $ 19 ou como dividir o servidor corretamente? (opções disponíveis com RAID1 e RAID10, até 24 núcleos e até 40 GB DDR4).
O Dell R730xd 2x é mais barato no data center Maincubes Tier IV em Amsterdã? Apenas temos 2 x Intel TetraDeca-Core Xeon 2x E5-2697v3 2.6GHz 14C 64GB DDR4 4x960GB SSD 1Gbps 100 TV a partir de $ 199 na Holanda!Dell R420 - 2x E5-2430 2,2 Ghz 6C 128 GB DDR3 2x960 GB SSD 1 Gbps 100 TB - a partir de $ 99! Leia sobre como construir a infraestrutura do prédio. classe com o uso de servidores Dell R730xd E5-2650 v4 a um custo de 9.000 euros por um centavo?