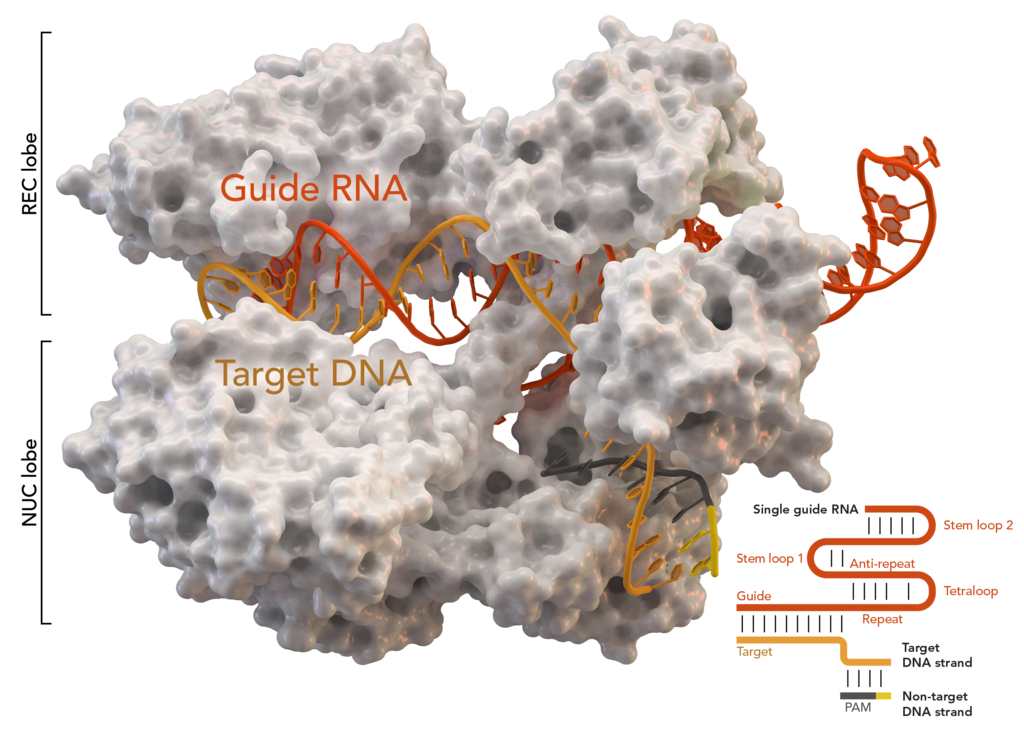
Estrutura cristalina de S. aureus Cas9 em um complexo com crRNA e seu DNA alvo
Em postagens anteriores você pediu para contar com mais detalhes sobre CRISPR / Cas9 e abordagens para edição de genoma. Só não incluí um material tão volumoso no último post. E nisso não incluirei, por exemplo, o método TALEN, que pode ser potencialmente mais preciso e tem suas vantagens. Mas querida, sim.
Vamos tentar percorrer o método já bem descrito de modificação genética usando CRISPR-Cas9 e olhar um pouco mais amplamente para as perspectivas que ele abre para nós. Eu estava extremamente interessado na direção do transplante xenogênico de porcos para humanos. O primeiro método de "pré-correção" mostrou que o transplante de porco é morto pelo corpo interno alguns minutos . Mas o método não foi descartado. Ainda assim, esta é uma maneira promissora de não esperar até que outro potencial doador de órgãos morra, mas de cultivá-los com antecedência. Descobriu-se então que os porcos também carregam um pacote de retrovírus específicos embutidos em seu genoma e podem causar uma epidemia de uma nova xenozoonose. E os vírus também devem ser detectados de alguma forma antes do transplante. E em algum lugar aqui aparecem pessoas de jaleco branco, fazendo algo incompreensível em seus laboratórios ...
O antivírus bacteriano que virou tudo de cabeça para baixo
Em 1987, o CRISPR foi descoberto por cientistas japoneses liderados por Yoshizumi Ishino. Naquela época, eles chamaram a atenção para as repetições incomuns no genoma de E. coli, mas não deram importância especial a isso. E somente quando repetições semelhantes foram encontradas em arqueas, que são geneticamente muito distantes de E. coli, é que eles começaram a procurar estruturas semelhantes em outros procariotos. Esses fragmentos são chamados de CRISPR - repetições palindrômicas curtas regularmente interespaçadas em cluster. Um pouco mais tarde, proteínas especiais associadas a CRISPR, Cas ( CRISPR como proteína associada), também foram descobertas. Bem descoberto e descoberto, ao que parece. Mas eles foram o início de uma nova revolução biotecnológica.
Agora vou tentar dizer como funciona e por que as bactérias precisam dele. A bactéria adoraria sobreviver. Mas eles gostam de parasitar vírus. Quando alguém te come - é desagradável e você tem que fazer algo. Como resultado, a resposta foi um mecanismo complexo, mas extremamente interessante. A bactéria armazena tremulamente em um pedaço de seu genoma as assinaturas de todos os vilões que estão tentando infectá-la. Estas são as mesmas regiões palindrômicas repetitivas - CRISPR. Eles trabalham em conjunto com proteínas do grupo Cas. Estamos interessados na chave Cas9. Como fica ao vivo, se um pouco simplificado?
Se esse sistema não funcionar, a célula bacteriana é incapaz de distinguir o genoma viral, cuidadosamente introduzido pelo bacteriófago, do seu próprio. E o sistema não muito inteligente de síntese de proteínas é imediatamente reorientado para a liberação de novas gerações de fagos. A célula morre.
Se CRISPR / Cas9 for acionado, o processo é diferente. A bactéria usa os dados registrados no CRISPR para criar RNA de controle. O complexo de proteínas começa a desenrolar o DNA para testes antes do "lançamento". Caso a sequência corresponda às assinaturas virais registradas no CRISPR, o Cas9 dispara o alarme e imediatamente corta o fragmento inimigo reconhecido. Ou seja, mesmo que um vírus esteja embutido no genoma bacteriano no nível de “firmware”, ele será removido de lá assim que o antivírus embutido o reconhecer.
premio Nobel
Emmanuelle Charpentier e Jennifer Doudna receberam o Prêmio Nobel de Química de 2020 pela criação de novas tecnologias que permitem ao CRISPR-Cas9 realizar a edição do genoma. Essa tecnologia tornou possível substituir os métodos mais precisos da época, porém mais complexos e caros, dos dedos de zinco e das nucleases TALEN. Os métodos anteriores exigiam o desenvolvimento, a expressão e a validação de um par de polipeptídeos completamente novo para cada novo locus alvo. E o CRISPR-Cas9 deu uma ferramenta padrão, quando usada na versão mínima, basta obter a sequência de controle necessária, de acordo com a qual Cas9 encontrará a área necessária para a dissecção.
Ok, cortamos o DNA de um humano, fermento ou rato de teste. Isso é legal, mas agora temos duas peças quebradas e uma corrente destruída. Existem várias opções para costurar de volta.

Você pode tentar combinar as peças cortadas usando o método de união de extremidade não homólogo. Ele está à direita. Para simplificar, nesta versão, estamos simplesmente tentando encaixar a quebra dupla diretamente e soldá-la em um único todo. Este mecanismo é bastante ineficaz, no processo de "encaixe" porções de extremidade individuais podem cair. Como resultado, pequenos fragmentos são freqüentemente perdidos na zona de quebra ou, ao contrário, inserções curtas aparecem. Essa abordagem geralmente desliga o gene de forma irreversível, tornando-o defeituoso.
A segunda opção é mais interessante. Ele está na ilustração à direita. O reparo por recombinação homóloga implica a substituição de uma sequência deletada por uma nova sequência complementar a um modelo de reparo criado pelo próprio pesquisador. Como resultado, é possível não apenas desligar o gene de alguma forma, mas substituir a sequência mutante pela normal.
O principal problema do método é que ele é probabilístico. Sim, em uma grande porcentagem dos casos, funcionará exatamente como deveria. Mas em muitas células, ele não dará o efeito desejado ou levará algo para o inferno. E é bom que apenas células isoladas morram disso, e não se tornem, por exemplo, células tumorais. Portanto, todas essas mudanças devem ser testadas exaustivamente. Felizmente, abordagens relativamente novas melhorar a especificidade criando um Cas9 personalizado pode reduzir o número de cortes errôneos a quase zero.
Xenoenxertos
Como eu disse antes, o uso massivo dessas técnicas interrompe a especificidade. Se nossa maravilhosa molécula simplesmente perder 20% das células, não é grande coisa. Isso significa que 80% das células humanas com mutação congênita estão fixas e já começarão a produzir a enzima correta, se dividir adequadamente ou fazer outra coisa corretamente. Via de regra, isso é mais do que suficiente para uma pessoa se tornar clinicamente saudável.
Nesta seção, gostaria de falar um pouco sobre como a edição do genoma pode potencialmente resolver o problema da doação de órgãos. Devo dizer que a falta de órgãos para transplante parece muito triste. Tempos de espera enormes e muitas questões éticas.
O número de transplantes de órgãos realizados na Rússia é centenas de vezes menorprecisa. Se o mesmo rim pode ser transplantado de um parente adequado, então um transplante de coração já significa a morte do doador. Uma das áreas-chave na busca por uma fonte ilimitada de órgãos é o xenotransplante. É uma opção para o transplante de tecidos e órgãos entre diferentes espécies. Um dos doadores mais adequados em estrutura e tamanho para humanos é um porco , por incrível que pareça. Os primatas, embora geneticamente mais próximos, geralmente são muito menores em tamanho e muito caros para se reproduzir. Infelizmente, os primeiros experimentos com transplantes de órgãos de suínos mostraram que eles começam a rejeitar com uma resposta hiperaguda poucos minutos após serem conectados à corrente sanguínea.
Como modificar um porco

Para que o transplante não seja rejeitado, é necessário pelo menos nocautear os genes-alvo responsáveis pela síntese das proteínas mais estranhas a nós. A primeira dessas proteínas é a enzima alfa-1,3-galactose, que em todos os primatas é irreversivelmente quebrada no curso da evolução. É ele quem causa o início da rejeição em poucos minutos . A correção do gene permitiu a criação de uma raça de porcoscom um gene desligado responsável pela síntese da enzima - GTKO de porco. Embora isso tenha desacelerado significativamente o processo de rejeição, não o interrompeu completamente. Descobriu-se que o ácido N-glicolilneuramínico e β1,4 N-acetil galactosaminiltransferase, que estão ausentes em primatas, também são problemáticos. Esses genes também foram nocauteados e os porcos GGTA1 / CMAH / β4GALNT2 KO foram obtidos com todos os três genes desativados ao mesmo tempo. Presumivelmente, isso pode praticamente neutralizar a reação de rejeição . Em teoria, se isso também forçar as células suínas a sintetizar a glicoproteína CD47 de superfície de uma pessoa, então a compatibilidade será excelente .
Houve uma publicação muito promissora em 2018 no transplante de coração de porcos OGM para babuínos. Dos 5 babuínos, apenas um teve problemas, o edema pulmonar começou por razões cirúrgicas e teve que ser retirado do experimento com antecedência. O restante sobreviveu até o final do período de experimento com boa saúde. Dois a três meses e dois a seis meses. Houve alguns problemas devido ao crescimento do órgão, já que o coração de um porco é maior que o de um babuíno, mas para uma pessoa isso não será um problema.
Existe um novo HIV à nossa frente?

Árvore filogenética do HIV e vírus relacionados em chimpanzés
Parece que um futuro brilhante nos espera, onde um rebanho separado de porcos de laboratório especiais pastará para a produção de órgãos de doadores. Mas também aqui surgem muitos problemas éticos. Suspeito que tal método seja inaceitável para representantes de várias religiões, o que automaticamente o torna inacessível para uma grande proporção da população mundial.
Os porcos também possuem retrovírus. Isso inclui, por exemplo, um lentivírus maravilhoso como o vírus da imunodeficiência humana e vírus de primatas relacionados. Acredita-se que foi o vírus primata que deu origem à maciça epidemia de HIV na década de 70 do século passado. E agora a pessoa não sabe o que fazer com ela. Os porcos são portadores de PERVs - retrovírus endógenos suínos. E você não pode se livrar desses vírus por meio de reprodução cuidadosa e medidas anti-epidêmicas, uma vez que os vírus já estão firmemente embutidos no genoma de suas células. A pesquisa foi conduzida que deve dar uma solução possível. Para começar, eles pegaram células de porco e as cultivaram na mesma cultura que as células embrionárias de um rim humano. O mais irritante é que conseguiram identificar células humanas infectadas com retrovírus suínos, o que potencialmente indica essa possibilidade de transplante. Como solução, propuseram o pré-processamento das células com CRISPR-Cas9 e a excisão completa de todos os fragmentos virais da cultura de células do epitélio renal porcino.
Biotecnologia e riscos
É difícil prever onde tudo isso vai levar. Infelizmente, os riscos de se obter um mutante viral exótico em tal transplante estão longe de ser zero. E há uma chance de que essa infecção também possa se espalhar silenciosa e imperceptivelmente, antes que se torne óbvia, como aconteceu em sua época com o HIV. Mesmo assim, estou bastante otimista. Iremos inevitavelmente pisar em muitos ancinhos no processo de pesquisa, mas agora temos as ferramentas para tratar doenças anteriormente fatais e prolongar a vida humana.
